noch mal das Thema Scheiden von Edelmetall, wieder das Versuchschemie-Forum nur dieses mal mit der freundlichen Erlaubnis von Florian. Wieder ein sehr Interessanter Einblich der uns auf diese Art ermöglicht wird. Wie die Edelmetallscheidung von Gold von statten geht könnt Ihr
nachlesen.
Verarbeitung von 925 Silber zu 999er SilberIm Folgenden möchte ich euch eine Möglichkeit vorstellen, um verunreinigtes Silber und altes Schmucksilber aufzuarbeiten.
Es wäre manchmal vielleicht von Vorteil, wenn man einen Magnetheizrührer hätte, jedoch geht es auch ganz gut ohne.
Geräte:Erlenmeyerkolben
Bechergläser
Schliffkolben
Rückflusskühler
Bunsenbrenner
Dreifuß
Keramikdrahtnetz
Glasstab
oder Magnetrührer
Glastrichter und Filterpapier
oder Büchnertrichter, Vakuumpumpe, Saugflasche, GuKo, und Filterpapier
Kochplatte
oder Magnetheizrührer mit Rührfisch
Öl/Wasserbad
eventuell Korkring
Chemikalien:Salpetersäure 65%
R: 35
S: 23.2-26-36 / 37 / 39-45
Salzsäure 20%
R: 34-37
S: 26-36/37/39-45
Natriumhydroxid
R: 35
S: 26-37-45
SaccharoseR: -
S: -
dest.WasserR: -
S: -
SilberQuelle: aus altem Schmuck, Löffelsilber, Krawattennadeln oder Manschettenknöpfen
Sicherheitshinweise:Achtung bei der Arbeit mit den Silbersalzen!
Wenn man Silberchlorid an die Finger bekommt, färben sich diese, über den Tag verteilt, erst weiß, dann violett und schließlich grau-schwarz, wenn die Fingernägel etwas abbekommen werden diese auch schön braun.
Auch wenn man sich die Hände nach der Arbeit wäscht, geht das Silberchlorid nicht weg.
Am Ende sind noch drei Wege beschrieben, wie man die Silberflecken entfernen kann
Bei der Oxidation von Silber zu Silbernitrat mit Salpetersäure bilden sich Stickoxide (NOx) welche sehr giftig sind! Versuchsdurchführung:
Versuchsdurchführung: 
1. Vom Silber zum Silberchlorid
2. Reinigung des Silberchlorids
3. Reduktion des Silberchlorids zu elementarem Silber
4. Einschmelzen des elementarem Silber
4.1. Möglichkeiten des Einschmelzens
4.2. Mögliche Behälter zum Einschmelzen
1. Vom Silber zum SilberchloridIn einem Erlenmeyerkolben kommen auf 1g Silber 2ml 65% Salpetersäure.
Dies sollte im Abzug oder im Freien geschehen, da giftige NOx entsteht.Zur Beschleunigung wird das Ganze mit dem Brenner leicht erhitzt.
Falls das Silber sich nicht mehr löst, das heißt keine Bläschen steigen mehr am Silber auf, wird noch etwas Salpetersäure hinzugegeben .

Wenn alles Silber gelöst ist, wird die Lösung etwa um die Hälfte verdünnt .Nun wird unter Rühren mit dem Glasstab oder dem Magnetrührer, 20% Salzsäure hinzugegeben.


Eventuell warten bis sich das Silberchlorid abgesetzt hat und dann noch einmal Salzsäure hinzugeben, um zu prüfen ob noch Silbernitrat gelöst ist.
Ich hatte den Fehler gemacht nicht zu verdünnen, dadurch hatte sich zuviel Silberchlorid in der Lösung gebildet, so dass ich erst noch einmal abfiltrieren mußte und dann erst das restliche Silberchlorid aus der Lösung holen konnte ===> VerlusteDann wird abgefiltert/abgenutscht. Die gefilterte Lösung wird noch einmal mit Salzsäure überprüft und eventuell abgefiltert.
2. Reinigung des SilberchloridsDer Filterrückstand kommt in einen Schliffkolben. Es wird soviel 20% Salzsäure hinzugegeben, bis das Silberchlorid bedeckt ist.
Wenn man keinen Magnetrührer hat, dann schüttelt man einmal durch oder rührt mit dem Glasstab um, danach wird (nach eventueller Zugabe eines Rührfisches) der Rückflusskühler aufgesetzt und man läßt es vor sich hin köcheln. Wenn die Salzsäure gelb-grünlich ist,
wird abdekantiert und neue Salzsäure hinzugegeben. Dies wird solange gemacht, bis sich die Salzsäure nicht mehr verfärbt.
Dann wird das Silberchlorid mit dest. Wasser ausgewaschen bis es nicht mehr sauer reagiert.
 3. Reduktion des Silberchlorids zu elementarem Silber
3. Reduktion des Silberchlorids zu elementarem SilberMan kippt in den Kolben eine gesättigte Saccharose-Lösung, etwa soviel bis das Silberchlorid grosszügig bedeckt ist (ich hatte es ein wenig übertrieben)und gibt jetzt solange festes Natriumhydroxid hinzu, bis keine Reaktion mehr stattfindet.
 Achtung bei der Reaktion erhitzt sich die Lösung sehr stark. Wenn ihr es auf einmal brummen hört, ist das nicht euer Magen sondern ebenfalls das Gemisch
Achtung bei der Reaktion erhitzt sich die Lösung sehr stark. Wenn ihr es auf einmal brummen hört, ist das nicht euer Magen sondern ebenfalls das Gemisch  .
.Das Silberchlorid sollte nun komplett zu grauem elementarem Silber reduziert sein.

Das elementare Silber wird nun mit dest. Wasser gewaschen, bis es nicht mehr alkalisch reagiert.
Nun muß das elementare Silber getrocknet werden.
1. Entweder im Exsikkator,
2. unter Vakuum,
3. oder man dampft es im Wasser/Ölbad ein.
Man sollte es nicht direkt mit der Brennerflamme eindampfen, da die Suspension zu zähflüssig ist und die Wärme sich nicht gleichmäßig verteilt. Dadurch kann der Kolben springen oder das elementare Silber spritzt sehr doll, daher ist das Wasserbad besser, da es gleichmäßig und mit niedriger Temperatur eingedampft wird.
Es wäre besser, wenn man das elementare Silber in ein Becherglas umgießt solange es noch eine Suspension ist, da es später ziemlich schwierig ist das trockene Silber aus dem Rundkolben rauszubekommen.

Jetzt sollte man trockenes und sauberes elementares Silber haben.
4. Einschmelzen des elementarem SilberNun muß das elementare Silber eingeschmolzen werden, hier ein paar Möglichkeiten :
4.1.1 BunsenbrennerMit dem Bunsenbrenner ist es leider nicht möglich, das elementare Silber einzuschmelzen.Ich habe es wohl nur mit einem Gas-Kartuschenbrenner probiert, jedoch auch mit einem Teclubrenner klappt es nicht, folglich diesem
.
4.1.2 Schweißgerät oder ähnlichesMit einem Schweißgerät oder anderem Brenner mit Sauerstoff/Luft-Zufuhr geht es ziemlich leicht, das elementare Silber einzuschmelzen, weitere Infos in dem gleichen
.
4.1.3 GebläseofenDie letzte Möglichkeit ist der Gebläseofen.
Die Anregung hab ich von Desinfector bekommen aus dem Experiment von
Ich hab mir dann halt so meine Gedanken gemacht und mir einen Gebläseofen aus Beton gegossen, obwohl alle meinten, der Beton hält die Hitze nicht aus.
Eigentlich hatten sie Recht, es hat Risse gegeben, aber der Gebläseofen ist nicht gesprungen, mit ein bisschen Lochband war die Sache dann aber wieder schnell repariert.
Die Anleitung für den Gebläseofen werde ich demnächst auch posten, aber hier schon einmal der ungefähre Aufbau und ein Bild des Gebläseofen, während dem Silber einschmelzen.
 4.2.1 Porzellantiegel
4.2.1 PorzellantiegelDie erste Portion habe ich in einem Porzellantiegel eingeschmolzen, was sogar ganz gut geklappt hat. Nachdem ich ihn aber rausgenommen hatte, habe ich gesehen, dass sich an der Unterseite kleine Silberkügelchen gebildet haben und der Tiegel Risse hatte.
Ich vermute aber, dass sich die Risse nicht wegen der Hitze gebildet haben, sondern weil ich den Tiegel zweimal auf kalte Steine abgestellt hab.

 4.2.2 Graphittiegel
4.2.2 GraphittiegelAm Besten ist es, das elementare Silber in einem Graphittiegel mit Deckel einzuschmelzen!
- es kommt kein Sauerstoff daran und es gibt keine häßlichen Spratzer
- der Graphittiegel ist hitzebeständig genug und kann nicht springen.
Die geschmolzene Perle wird noch ein letztes Mal in 20% Salzsäure ausgekocht, um eine glänzende Oberfläche zu erhalten.
Ausbeute:Kann ich leider nicht sagen, da ich vergessen hatte das Silber zu wiegen und ich noch nicht alles Silber eingeschmolzen hab. Ich schätze jedoch, dass ich etwa 50% Verlust gemacht habe, wegen dem vielen Ausprobieren.Hier sind es schon einmal 7,3 g.
 Erklärung:
Erklärung:Das Silber wird von der Salpetersäure zu Silbernitrat oxidiert, welches in der Salpetersäure gelöst vorliegt.
Ag + 2 HNO<sub>3</sub> ===> NO<sub>3</sub><sup>-</sup> + NO<sub>2</sub> + H<sub>2</sub>O
Mithilfe der Salzsäure wird das Silbernitrat zu Silberchlorid ausgefällt.
AgNO<sub>3</sub> + HCl ===> AgCl (s) + HNO<sub>3</sub>
Das mit Natriumhydroxid alkalisch versetzte Silberchlorid wird mit einer Saccharose Lösung zu elementarem Silber reduziert.
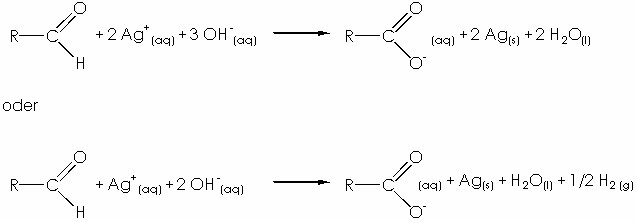 Fazit:
Fazit:Da ich leider keine vollständige Vorschrift hatte, habe ich mir die Sachen aus dem Forum, Schulbuch und dem Internet zusammengesucht.
Ich hab wohl um die Hälfte an Verlusten einstecken müssen, jedoch hat es dafür viel Spaß gemacht, auszuprobieren und selber darüber nachzudenken.
Die Erklärung musste ich mir aus dem Internet und Schulbuch zusammenschustern, ich würde gerne selber eine Erklärung formulieren, jedoch fehlt mir leider noch das nötige Wissen. Daher möchte ich euch bitten, mich bei der Erklärung zu verbessern und zu ergänzen.
Vier Lösungen um Silberflecken auf der Haut zu entfernen1. Die Erste Möglichkeit ist die Flecken mit einer Kaliumiodid Lösung zu behandeln,
2. oder wenn man kein Kaliumiodid hat :
Silberflecken erst mit Iodlösung behandeln, anschließend mit Natriumthiosulfat-Lösung
(Umwandlung von Silber in Silberiodid, anschließend Bildung des löslichen Thiosulfatkomplexes).
Wenn der Silberfleck sich von schwarz nach gelblich verfärbt hat, hat die Iodierung funktioniert, und man kann zum Thiosulfat greifen....
4.Die letzte und billigste Möglichkeit, wenn man 1. und 2. nicht zur Verfügung hat, hilft nur noch viel Geschirr waschen und baden. Nach ein paar Tagen nutzen sich die Silberflecken ab und man kann sie teils mit der Pinzette abziehen oder mit der Bürste abschrubben. Nur die Flecken auf den Fingernägeln gehen nicht weg.
Ich denk aber, wenn man dem/der Apotheker/in die Hände unter die Nase hält, verkaufst sie einem auch mal 10g Iod/Kaliumiodid.
Zum Schluß noch eine Entdeckung die ich beim Ausprobieren machte: Im Internet stand, dass das Silberchlorid mit NaOH alkalisch versetzt werden soll, ich hatte mir dann gedacht, alkalisch wird es ja auch mit Ammoniak. Daher hab ich in ein Reagenzglas zu etwas Silberchlorid 10% Ammoniak-Lösung und eine gesättigte Sacharose-Lösung gegeben. Erst ist nichts passiert, dann habe ich das Gemisch im Reagenzglasständer stehen gelassen. Später hatte ich das Reagenzglas wieder in der Hand gehabt um das Silberchlorid abzufiltrieren, aber dann hatte ich auf einmal gesehen, dass sich ein Silberspiegel gebildet hat.



.
Später habe ich aber gelesen, dass sich in ammonikalischen Silberlösungen das explosive Silberamid –imid und –nitrid bilden kann.Da hatte ich mich dann nicht mehr so gefreut.


(auf dem Foto sind auch noch einmal die schwarzen Silberhände zu erkennen).
Vielen Dank ebenfalls an Tojojo für seine engagierte Mitarbeit an diesem Experiment.
Quellen:
Schulbuch
http://www.wikipedia.dehttp://www.versuchschemie.dehttp://www.philippzilles.de/chemie/vers ... ilber.html...Florian


























